PCR이 왜 이미 놀라울 정도로 최적화된 기술인지, 더 빠른 중합효소와 광학적 가열 방식의 가능성과 한계, 그리고 저가 실험실 장비가 확산되기 어려운 이유를 살펴본 글.
생물학에 관해 씁니다.
I.
글쓰기는 발견의 행위다. 때로는 특정한 주장을 하겠다는 마음으로 자리에 앉지만, 더 깊이 조사해보면 그 주장이 엉터리여서 검토를 견디지 못한다는 사실을 알게 된다! 글쓰기에는 자신의 논리 속 구멍을 드러내는 아름다운 성질이 있는데, 이 에세이도 그랬다.
처음에는 중합효소 연쇄 반응, 즉 PCR이 1987년 첫 “현대적” thermocycler 기계가 출시된 이후 사실상 거의 바뀌지 않았다는 점을 길게 주장하는 글을 쓰려 했다. 논지는 PCR을 훨씬 더 빠르고, 더 싸고, 더 좋게 만들 방법이 분명 많이 있어야 한다는 것이었다. 이 주장은 대체로 맞지만, 내가 예상했던 정도는 아니다. 새로운 PCR 기술로 얻을 수 있는 시간 절감은 크지 않고, 과학자들은 몇 가지 이유 때문에 싼 PCR 기계를 사는 데 주저한다. (이 점은 뒤에서 더 이야기하겠다.)
그럼에도 이 글은 여전히 쓸 가치가 있어 보였다. 계기는 Fast Biology Bounties에 제출된 두 가지 아이디어, 즉 Sebastian Cocioba와 “Utah” Hans가 제안한 광학적 PCR 기계 구상에서 나왔다. 광학적 PCR의 요지는 LED 조명이나 레이저를 이용해 샘플을 빠르게 가열함으로써, 40회의 DNA 증폭 사이클을 6분 안에 수행할 수 있다는 것이다. 나는 Astera Institute의 후원으로 이 아이디어들을 지원하기 위해 3,500달러의 마이크로그랜트를 지급했다.
더 빠른 PCR은 얼핏 보기에 그렇게 매력적인 문제처럼 느껴지지 않을 수도 있다. 하지만 몇 가지 이유로 중요하다. 첫째, 널리 쓰이는 방법이 조금만 개선되어도 과학 전체의 생산성에 엄청난 하류 효과를 낼 수 있다. 둘째, 더 많은 생물학 실험이 자동화되고 로봇이 24시간 내내 이 실험들을 수행하게 되면, 이런 시간 개선 효과는 기하급수적으로 확대될 것이다. PCR에서 20분을 줄이는 일은 인간 과학자에게는 큰일이 아닐 수 있지만, 로봇에게는 매우 중요할 수 있다!
하지만 알고 보니 내가 느슨하게나마 갖고 있던 여러 가정이 금세 뒤집혔다. 광학적 PCR이 아무리 흥미로워 보여도, 이것이 가까운 시일 내에 학술 연구실에 등장할 가능성은 낮다고 생각한다.
이메일을 입력하세요…
구독하기
II.
PCR은 DNA를 복제하는 수십 년 된 방법이다. 수백만 명의 생물학자들이 거의 매주 이를 사용하며, 유전자 클로닝부터 질병 진단까지 온갖 일에 활용한다. 작동 방식도 꽤 단순하다. 작은 튜브를 하나 준비해 복제할 DNA 서열, 즉 복사할 분자를 넣는다. 다음으로 DNA 중합효소와 프라이머를 넣는데, 프라이머는 복제할 DNA 서열에 결합하는 짧은 DNA 조각이다. 마지막으로 뉴클레오타이드(DNA의 원재료)와 마그네슘을 넣는다. 그런 다음 그 튜브를 대략 DVD 플레이어 정도 크기의 기계인 thermocycler 안에 넣는다. 이 기계의 유일한 역할은 온도를 반복해서 올리고 내리는 것이다.
기계는 먼저 온도를 약 96°C까지 올려 이중 가닥 DNA 분자를 녹이고, 이를 두 개의 분리된 조각으로 만든다. 그다음 온도는 60°C로 떨어지는데, 이는 프라이머가 DNA 분자에 달라붙기 완벽한 온도다. 이어서 장치는 다시 약 70°C로 올라가는데, 이 온도에서 중합효소가 가장 활발하게 작동한다. 각각의 중합효소는 프라이머를 찾아 붙잡고, 뉴클레오타이드를 이어 붙이면서 DNA를 복제하기 시작한다. 마지막으로 thermocycler는 다시 96°C로 돌아가 새 사이클을 시작한다. 이 사이클이 한 번 돌 때마다 튜브 속 DNA 양은 대략 두 배가 된다. 보통 단일 PCR 실험에는 30개의 사이클이 있으며, 이는 두 가닥의 DNA가 (완벽한 효율을 가정하면) 2 30개의 복사본, 즉 10억 7천만 개의 분자가 된다는 뜻이다.
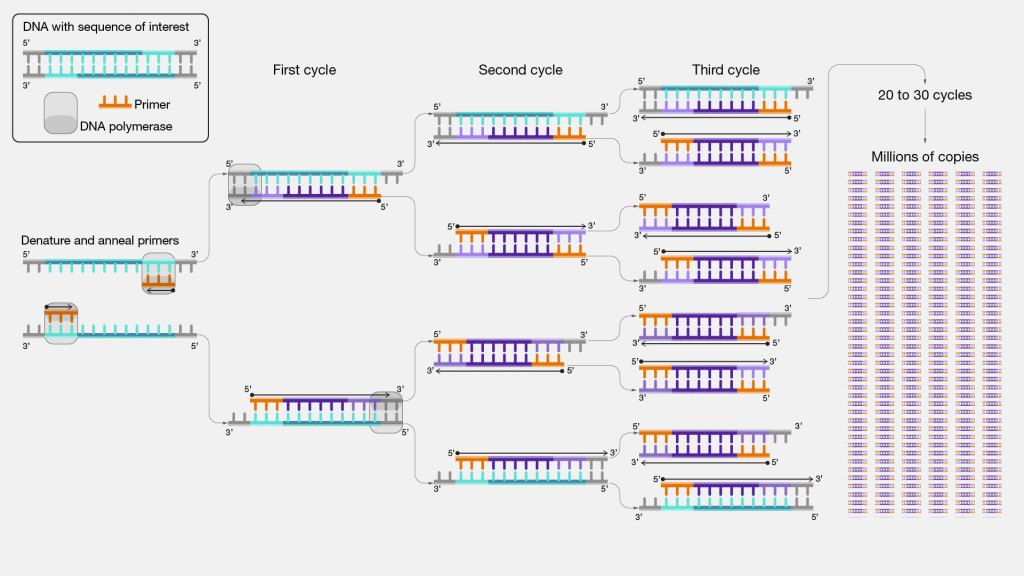
PCR의 작동 원리. 출처: genome.gov.
오늘날 PCR을 한 번 돌리는 데는 약 한 시간이 걸린다. 각 사이클에는 몇 분이 걸린다. 왜 이것은 훨씬 더 빨라질 수 없는 걸까?
여기에는 세 가지 요인이 있다. 확산, 즉 분자들이 올바른 위치로 이동하는 데 걸리는 시간, 복제되는 DNA의 길이, 그리고 각 온도 사이의 램프 속도다. 확산이 중요한 이유는 프라이머와 중합효소가 표적을 “찾기” 전까지는 DNA가 복제될 수 없기 때문이다. 더 긴 DNA 가닥은 중합효소가 일정한 속도(초당 약 60개의 뉴클레오타이드)로 움직이기 때문에 복제에 더 오랜 시간이 걸린다. 램프 속도는 thermocycler가 예를 들어 96°C에서 70°C로 식어야 한다는 뜻일 뿐이다. 이 모든 데 시간이 든다.
하지만 이런 요인들을 염두에 두면, 이런 병목을 줄일 방법을 생각해볼 수 있다.
PCR을 빠르게 만드는 가장 쉬운 방법은 사이클 수를 줄이는 것이다. 대부분의 과학자는 기본값으로 30사이클을 사용하지만, 여기에 특별한 이유가 있을까? 아마도 PCR 혼합물 속 일부 성분(프라이머나 뉴클레오타이드 같은 것들)은 30사이클 이전 에 바닥나므로, 마지막 몇 사이클은 사실 큰 의미가 없을 것이라고 생각할 수 있다.
하지만 꼭 그렇지는 않다! PCR 혼합물 속 일부 성분은 사이클 사이에 재사용되지만(예를 들어 중합효소), 다른 성분은 DNA가 만들어질 때마다 소비된다. 예를 들어 프라이머는 새로운 가닥에 물리적으로 편입되고, 뉴클레오타이드는 이를 만드는 데 사용된다. 하지만 이들 성분 중 어느 것도 30사이클 전에 바닥나지 않는다. 50마이크로리터 PCR 튜브에는 각 뉴클레오타이드가 약 6 × 10¹⁵개 분자 들어 있으며, 3,000염기 유전자의 복사본을 10¹²개 이상 만들기에 충분하다. (비교를 위해 말하면, 10¹²는 2 30보다 1,000배 크다.) 프라이머와 중합효소도 제한 요인이 아니다. 중합효소는 약 35사이클이 지나야 비로소 부족해지기 시작한다.
PCR의 실제 한계는 “product reannealing”이다. 이는 DNA 복사본이 더 많아질수록(수억 개 수준에 이르면) annealing 단계 동안 프라이머가 결합하기 전에 DNA 복사본들이 서로를 더 빨리 찾아 결합하기 시작한다는 뜻이다. 증폭된 DNA가 프라이머와 경쟁하기 시작하면, 각 사이클의 효율은 떨어진다. 따라서 PCR을 30사이클에서 25사이클로 줄이면 단지 DNA 수율만 낮아질 것이고, 이는 이후 후속 실험이 잘 될 가능성도 낮춘다. 따라서 나는 PCR 사이클 수를 줄이는 것이 시간을 절약하는 좋은 방법이라고는 생각하지 않는다.
PCR을 빠르게 하는 두 번째 방법은 더 빠른 중합효소를 만드는 것이다. Taq 는 Yellowstone National Park의 거의 끓는 물에서 발견되는 “열을 좋아하는” 세균 Thermus aquaticus 에서 분리된 중합효소로, 초당 약 60개의 뉴클레오타이드 속도로 DNA를 복제한다. 이론적으로는 3,000염기 DNA 서열을 1분도 안 되어 복제할 수 있다. 하지만 현실에서는 중합효소가 DNA에서 계속 “떨어져 나가기” 때문에(정말로 거의 1초마다) 실제 속도는 훨씬 느리다. (Taq 를 판매하는 회사인 New England Biolabs는 DNA 1킬로베이스당 1분의 extension 시간, 즉 3,000염기에는 3분을 권장한다.) 70°C에서의 DNA extension 단계는 PCR에서 압도적으로 가장 긴 부분이다.

과학자들은 Taq가 발견되기 전에는 매 사이클마다 튜브에 “새” 중합효소를 추가해야 했고, 이를 위해 세 가지 서로 다른 온도로 유지된 물중탕 사이를 수동으로 옮겨야 했다.

최초의 “현대적” thermocycler인 TC1은 1987년 Perkin-Elmer와 Cetus에 의해 출시되었다.
Phusion 같은 다른 중합효소는 훨씬 더 빠르다. DNA를 따라 더 빨리 움직여서가 아니라, 그렇게 자주 떨어져 나가지 않기 때문이다. Phusion은 작은 DNA 결합 단백질인 Sso7d를 Pyrococcus 중합효소에 붙여 만든 공학적으로 설계된 단백질로, 이 덕분에 DNA 가닥을 더 단단히 붙잡는다. Phusion을 만든 회사 ThermoFisher는 extension에 킬로베이스당 단지 15초만 권장한다. 즉, 중합효소 하나를 다른 것으로 바꾸는 것만으로도 PCR 시간에서 한 시간 이상을 절약할 수 있다. 이는 이미 엄청난 시간 절감이며, 더 빠른 중합효소를 공학적으로 만들어도 아마 얻을 수 있는 것은 미미한 시간 절감뿐일 것이라고 나는 회의적으로 본다.
마지막으로 더 빠른 thermocycler를 만들면 PCR을 빠르게 할 수 있다. 현대 기계는 느리고 구식이다. 몇 년 전 ThermoFisher는 여러 thermocycler를 사서 샘플을 얼마나 빨리 가열하고 냉각하는지 직접 비교했다. 이 장비들에서 평균 상승 램프 속도는 4.75 °C/s였고 평균 냉각 속도는 3.82 °C/s였다. Bio-Rad T100 같은 더 저렴한 기계는 램프 속도가 2.5°C/s에 더 가깝다. (그리고 이런 기계들이 연구실에서 가장 흔하다.) 실제로는 온도를 바꾸는 데 시간이 꽤 많이 든다! 기계가 95°C에서 60°C로 떨어질 때마다 약 10초가 걸린다.
thermocycler도 지난 40년 동안 크게 달라지지 않았다. 보통은 큰 금속 블록 하나가 있는데 — 알루미늄이거나, 돈을 더 내면 은이다 — 여기에 튜브를 꽂기 위한 구멍이 뚫려 있다. 뚜껑이 내려오면 블록 위에 가열 요소를 밀착시키고, Peltier 소자가 전류를 흘려 한쪽을 덥히고 다른 쪽을 식힘으로써 블록을 가열한다. 온도를 바꾸려면 기계는 전류 방향을 뒤집고 팬이 남는 열을 날려 보낸다. 램프 속도가 느린 이유는 기계가 큰 알루미늄 덩어리의 열질량과 싸우고 있기 때문이다. 이 덩어리는 갑작스러운 온도 변화를 잘 버틴다.
그렇다면 PCR을 더 빠르게 만들기 위해 남은 진짜 선택지는 램프 속도를 크게 높이는 것뿐이다. 사이클을 줄이는 것은 별로 통하지 않고, 중합효소는 이미 너무나 아름답게 최적화되어 있어서 추가적인 이득은 작을 것이다. 하지만 레이저와 LED 조명은 어쩌면 램프 속도를 거의 즉시 수준으로 만들 수 있다. 그건 어떻게 가능할까?
III.
사람들은 수십 년 동안 LED와 레이저를 이용해 PCR을 해왔지만, 내가 알기로 상용화된 설계는 없다. 요지는 큰 알루미늄 블록을 가열하는 대신 액체 방울에 직접 빛을 비춰 가열할 수 있다는 것이다. 방울이 충분히 작고 표면적 대 부피 비가 높다면, 빛을 끄는 순간 그 열은 빠르게 흩어져 방울이 식는다. (팬도 필요 없다.)
2009년 논문에서 연구자들은 PCR 혼합물의 아주 작은 방울을 만들어 증발을 막기 위해 광유에 떨어뜨렸다. 그리고 방울을 58°C로 유지되는 유리 슬라이드 위에 올려놓았는데, 이 온도는 annealing과 extension 모두에 사용되었다. 그다음 위에서 적외선 레이저를 비춰 denaturation 단계에 필요한 93°C까지 방울을 가열했다. 물은 적외선을 강하게 흡수하는 반면 광유는 약 40배 덜 흡수하므로, 레이저는 물만 가열하고 다른 것은 가열하지 않는다. 레이저가 꺼지자마자 열은 빠르게 물에서 주변 기름으로 빠져나간다.
한 실험에서 연구자들은 이 장치를 이용해 187염기쌍짜리 DNA 가닥을 증폭했고, 약 6분 만에 40사이클을 끝냈다. 부피가 매우 작고 램프 속도가 매우 빨랐기 때문에, 각 사이클에는 denaturation 2초, primer annealing 1초, extension 7초만 있으면 되었다! (extension 단계만으로도 전체 시간의 약 3분의 2를 차지했다.) 레이저를 구동하는 데 필요한 전력도 아주 작아서, 전구보다 약 3,000배 적은 에너지를 소비한다.
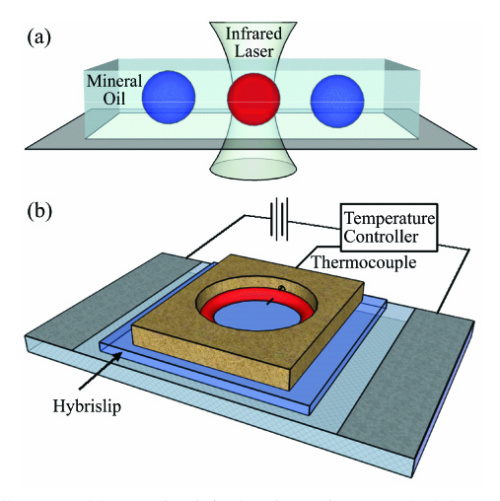
작은 방울을 가열해 PCR을 수행하는 적외선 레이저 방식. 2009년 논문에서.
2015년에는 UC Berkeley 팀이 비슷한 아이디어를 발표했는데, 레이저 대신 LED와 얇은 금막을 사용했다. 그들은 작은 플라스틱 조각을 금막으로 코팅한 뒤 그 위에 액체를 떨어뜨렸다. 그런 다음 아래쪽에 파란 LED를 두어 금을 가열하고, 그 열로 다시 그 위의 액체를 가열했다. (금은 빛을 효율적으로 흡수할 뿐 아니라 비활성이어서 PCR을 망치지 않기 때문에 이상적이다.) 이 단순한 장치로 그들은 55°C와 95°C 사이를 오가며 30사이클의 가열과 냉각을 약 6분 만에 수행할 수 있었다. 램프 속도는 시판되는 어떤 thermocycler보다도 약 두 배 빨랐다.
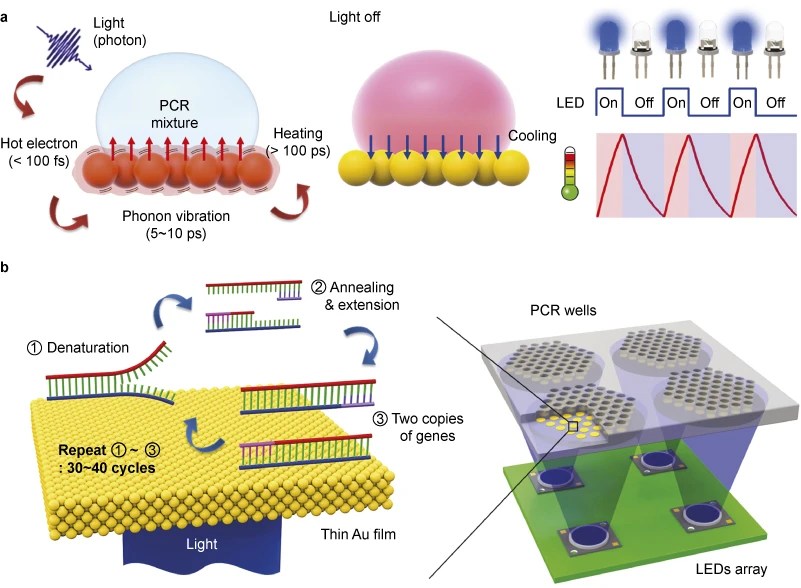
금막과 LED를 이용해 PCR을 하는 방식. 2015년 논문에서.
내가 지급한 두 개의 마이크로그랜트는 바로 이 선행 연구들에 직접적으로 기반한 아이디어였다. Sebastian Cocioba는 검은 PCR 튜브와 작은 레이저를 사용해 샘플을 가열하는 소형 장치를 만들고 있고, “Utah” Hans는 (대체로) 2015년 연구를 재현하면서 금과 LED 조명을 이용해 50달러 이하의 PCR 기계를 만들고 있다.
처음에는 이 아이디어들에 흥분했지만, 지금은 광학적 PCR이 널리 채택될 것이라고는 더 이상 확신하지 않는다. (값싼 프로토타입이 나와도 말이다.) 내 근거는 단순한 계산에서 나온다. 앞서 언급한 온도 조건 — 98°C (denaturation, 10초) → 60°C (annealing, 20초) → 72°C (extension, 45초) — 에서 Phusion 효소로 3,000염기 DNA로 이루어진 유전자를 증폭한다고 상상해보자. 시판 장비의 “평균적인” 램프 속도로는 얼마나 걸릴까? 그리고 램프 속도가 즉시라고 가정하면 얼마나 걸릴까?
둘 사이에는 큰 차이가 없다! 이 시나리오에서 온도 램핑만으로 사이클당 약 20초, 총 10분이 걸리며, 전체 PCR 시간의 약 20퍼센트를 차지한다. 따라서 램핑이 즉시 이루어진다 해도 큰 차이는 없다. PCR은 한 시간짜리 작업에서 50분짜리 작업이 될 뿐이다. 이것은 내게 꽤 놀라웠고, 광학적 PCR 장치가 널리 퍼지지 않은 이유를 부분적으로 설명해준다고 생각한다.
IV.
그렇다면 광학적 PCR은 시간을 많이 절약해주지 못한다. 하지만 누군가 실제로 작동하는 광학적 PCR 기계를 만들어 150달러에 판다고 해보자. (Utah는 나에게 여러 영상을 보내왔고, 제작비가 단 48달러인 작동 프로토타입도 가지고 있다.) 과학자들은 이걸 살까?
서류상으로는 그렇다! 일반적인 thermocycler는 가격이 2,500달러(저가형)에서 10,000달러(화려한 제어 장치와 터치스크린이 많은 경우)까지 간다. eBay에서 가장 싼 thermocycler는 230달러인데, 1997년 제품이다. 이 가격은 터무니없다. 다시 말하지만 thermocycler는 지난 40년 동안 거의 변한 것이 없기 때문이다. 그러니 서류상으로는 150달러짜리 광학적 PCR을 파는 일이 쉬워 보여야 한다.
하지만 값싼 실험실 하드웨어는 이전에도 시도된 적이 있고, 결과는 고무적이지 않다. 2010년, Tito Jankowski라는 바이오해커는 저가 thermocycler를 만들고, 시험하고, 판매하는 것을 목표로 한 비영리 단체 OpenPCR를 공동 설립했다. 각 장치는 제작비가 약 250달러였고 (놀랍게도 알루미늄 블록은 약 15달러밖에 들지 않았다) 500달러에 판매되었다. 그들은 결국 약 천 대의 기계를 팔았고, 지금 이 프로젝트는 종료되었다.

2011년경의 OpenPCR 장치.
Tito가 PCR 기계를 팔기 전에, 그는 블루 라이트 일루미네이터를 만들어 배송했다. 전기영동 후 젤을 시각화하고 “DNA를 보는” 데 쓰는 바로 그 조명이다. 이런 블루 라이트는 대기업 제품이 약 2,500달러였지만, Tito는 10달러 정도면 만들고 100달러에 팔 수 있다고 생각했다. 그래서 실제로 그렇게 했지만, 과학자들은 그 조명을 사고 싶어 하지 않았다. 상용 제품과 거의 똑같고 가격은 약 25분의 1이었는데도 말이다. 너무 싸면 뭔가 문제가 있을 거라고 과학자들이 생각했다는 것이다. Tito에 따르면, 가격을 두 배로 올리자 판매가 늘었다.
Tito는 같은 논리가 PCR 기계, 아니 사실상 어떤 실험실 하드웨어에도 적용된다고 생각한다. 과학자들은 데이터가 똑같이 잘 작동한다고 보여주어도 값싼 대안을 항상 신뢰하지는 않는다. 또 과학자와 엔지니어 사이에는 간극도 있다. 과학자들은 익숙하지 않은 장치에서 프로토콜 문제를 직접 해결해야 할까 봐, 혹은 실험이 더 이상 작동하지 않을까 봐 걱정하는 경우가 많다. 반면 엔지니어들은 하드웨어를 직접 실험하거나 스스로 만드는 일에 더 개방적이다.
따라서 문제는 가격만이 아니다. 전환 비용도 있다! 새로운 도구가 과학자들이 이미 알고 있는 것에서 멀어질수록, 채택될 가능성은 낮아진다. Taq 를 Phusion으로 바꾸는 것은 전환 비용이 낮다. 과학자들은 서로 다른 thermocycler를 쓰거나 프로토콜을 바꿀 필요 없이, PCR에서 효소 하나만 다른 것으로 바꾸면 되기 때문이다. 그리고 시간 절감도 크다.
연구실에 기존 워크플로를 버리고 레이저와 기름 방울로 바꾸라고 요구하면서, PCR 시간 20퍼센트 절감을 제시하는 것은 아마 통하지 않을 것이다. 코어 시설이나 대규모로 이를 운용하고 문제를 해결할 수 있는 로봇 연구실 같은 일부 그룹은 도입할 수 있겠지만, 대부분의 그룹에는 전환 비용이 너무 크고 장점은 너무 작다.
이 모든 것에는 고통스러운 아이러니가 있다. thermocycler는 수천 달러씩 하고 수십 년째 변하지 않았는데, 더 싸고 약간 더 빠른 대안조차 여전히 확산되기 어렵다. 도구가 일단 흔해지면, 그것은 깊이 자리 잡아 밀어내기 어려워진다. 오픈소스 또는 저가 실험실 하드웨어를 만드는 사람이라면 이 점을 꼭 염두에 두어야 한다.
JM: 오늘 당신의 PCR 블로그 글을 읽었는데, 내가 보기에 당신이 간과한 한 가지는 더 맞춤형이어야 한다는 점입니다.
당신이 지적했듯이, DNA 길이는 extension 시간을 결정합니다. 하지만 이것은 길이가 서로 다른 PCR들을 96웰 플레이트 하나에서 동시에 수행하고 싶을 때 문제를 일으킵니다. (우리 작업에서는 흔한 일입니다. 우리는 주문 후, 그리고 goldengate 전에 첫 단계로 PCR을 해서 짧은 조각의 goldengate 효율을 높입니다.) 현재 우리는 플레이트를 비슷한 길이끼리 나누거나 (합성 주문 단계에서 혹은 받은 후에) 대충 모두에 맞는 하나의 extension 시간으로 돌리려 합니다. 그래서 우리는 icon96을 검토해왔는데, 이 장비에서는 기계의 각 “웰”을 개별적으로 제어할 수 있어서 하나의 실험용기 안에 있으면서도 웰별 최적화가 가능합니다. 서로 annealing 온도가 다른 프라이머 세트를 하나 이상 쓰고 싶을 때도 장점이 있습니다. 마지막으로, 사이클 수와 관련한 흥미로운 혁신도 있습니다. 시작 물질과 무관하게 특정 DNA 농도에 도달하면 멈출 수 있도록 형광 염료를 추가했습니다. 이렇게 하면 후속 응용을 희생하지 않고도 사이클 시간을 줄일 가능성이 있습니다.
요컨대, 이들은 단일 웰 수준에서 즉석 프로토콜 최적화를 제공하는 것 같습니다.
HL: 시스템 수준 공학이 없으면, 생물학적 프로세스와 하드웨어, 그리고 생태계는 개선에 저항적일 것입니다.
PCR 자체는 분명 더 빨라질 수 있습니다. 사이클을 줄이면 됩니다. 맞춤형 NGS를 위한 qPCR 증폭을 하는 사람들은 30사이클보다 한참 아래에서도 거의 포화 상태에 도달하는 것을 볼 수 있습니다. 간과된 질문은 얼마만큼의 산물이 충분한가입니다. 우리는 흔히 너무 많은 양을 갖게 됩니다. 시작 물질은 얼마나 되었나요? 입력량과 프라이머 농도의 비율은 무엇인가요?
시스템 전반에 걸친 겉보기엔 사소한 개선들이 모이면, 특히 자율 실험실의 시대에는 생산적인 결과를 낳을 것입니다.
SD: 아마 회의적인 과학자들의 마음을 얻는 효과적인 방법 하나는 저가 장비를 무료로 써보게 하는 것일 수 있습니다. (예를 들어 1년 동안.) 이런 기계의 낮은 생산 비용을 생각하면, 이런 접근은 충분히 실행 가능해 보입니다.
MS: DNA 자체의 길이가 아니라, 중합효소의 속도입니다. 생물학은 자기 나름의 속도로 작동합니다. 그리고 중합효소의 최적 속도는 이미 잘 규명되어 있습니다. 램프 속도는 흥미롭습니다. 모세관 튜브(더 얇은 부피 단면) 안에서 뜨거운 공기 순환기(외부 온도 변화는 즉시)를 사용해 PCR을 하면 그것을 더 빠르게 할 수 있고, 실제로 그렇게 한 사례도 있습니다. 예를 들어 Roche의 초기 LightCycler는 30분이 걸렸습니다.
하지만 32샘플 모세관 시스템은 뜨거운 공기로는 확장되지 않습니다. 최적화 대상이 잘못되어 있었던 셈입니다. 연구실은 종종 96웰 플레이트뿐 아니라 384웰 플레이트까지 처리량을 확장하고 싶어 합니다. 시간이 두 배 걸리더라도 샘플을 10배 더 처리할 수 있다면, 왜 사이클 시간을 절반으로 줄이는 데 신경을 쓰겠습니까? PCR이 돌아가는 동안 연구실에서 할 다른 일이 없는 것도 아니니까요.
RA: 공학적으로 설계된 중합효소가 5s/Kb 속도까지 나온다면, 효소 수율이 병목인지는 잘 모르겠습니다. 효소는 여전히 떨어져 나와야 하고, 프라이머는 anneal해야 하며, 효소는 다시 template를 찾아야 합니다. 반응도 시간이 지나면서 자기 억제됩니다.
어쩌면 완전히 다른 방식으로 생각해야 할지도 모릅니다. 예를 들어 매우 높은 온도에서 작동해 strand displacement가 필요 없는 rolling circle polymerase가 있을 수 있습니다. template가 각 nt extension 직후 바로 해리되기 때문이죠. 그건 매우 빠를 수 있습니다. 혹은 DNA 산물과 반응 성분의 양을 동적으로 제어하는 방법, 예를 들어 채널을 계속 혼합하는 microfluidic 장치라면 포화 문제를 다루고 반응을 지속적으로 지수적으로 유지할 수 있을 것입니다. 또는 template를 한 번 복사하는 대신 각 사이클마다 병렬로 여러 복사본을 만드는 마법 같은 중합효소도 가능할지 모릅니다. (예를 들어 서로 다른 위치에서 동시에 뉴클레오타이드를 더하고, 일반적인 증폭과 strand displacement를 조합해 증폭하는 식입니다.) 혹은 concatemerised template에서 rolling circle을 수행해 매 사이클마다 초기 template의 2배 이상을 만들 수도 있겠죠… 즉, 브레인스토밍하고, 버릴 건 버리고, 금을 남길 아이디어들입니다.
EM: 2014년에 첫 PCR을 세팅하던 게 기억나네요. DNTP랑 이런저런 것들을 다 넣어야 해서 엄청 오래 걸렸어요. 진짜 악몽 같고 짜증났죠. [Master Mix]의 효율 향상은 엄청났습니다…. 임상적으로 생각해보려 하는데, 여기저기 한 시간 정도가 차이를 만들 만큼 PCR이 시간 민감한 상황이 있는지는 잘 모르겠습니다. 세균 감별에는 기억하기로 MALDI-TOF를 쓰고, 감수성 검사 같은 것도 그렇고, PCR은 특정 생물체를 식별할 때 쓰이기도 합니다. (대변, 요도 면봉 등) 하지만 이런 경우들도 대개는 경험적 치료가 먼저 시작됩니다.
MPS: 광학적 PCR은 qPCR에 꽤 잘 맞을 수도 있겠습니다. qPCR은 보통 형광으로 읽어내니, 광학계가 통합되어 있으면 도움이 될 테니까요. 또는 ddPCR에도요.
PC: 흥미로운 글입니다. 이제는 extension 시간에 투입되는 반응 비율을 줄일 수 있을 만큼 훨씬 더 빠른 중합효소들이 있습니다. (우리는 Repliqa를 쓰는데 최대 1s/kb까지 나옵니다.) 그러면 램프 속도 절감의 비중은 비례적으로 더 커질 수 있겠죠.
FC: MBS/NextGenPCR 같은 회사들이 SBS 형식 플레이트로 무엇을 해왔는지 살펴볼 만합니다. (예: 3 temp 40 cycle PCR을 2분에 수행) PCR을 꽤 더 빠르게 만드는 방법은 많습니다. 특히 qPCR에서 그렇습니다. (반응 후 물질에 접근해야 한다면 선택지는 꽤 달라지겠지만요.) 긴 amplicon에 대해서도 마찬가지입니다. 그리고 효소 공학에는 엄청난 기회가 있을 가능성도 충분합니다. (Roche 사람들은 이 분야에서 놀라울 정도입니다.)
좋아요 로딩 중…
최신 글을 이메일로 받아보려면 구독하세요.
이메일을 입력하세요…
구독하기
2026.04.22
←이전
Indice –––––––––
Niko <3
지금 구독하고 계속 읽으며 전체 아카이브에 접근하세요.
이메일을 입력하세요…
구독하기
구독하기
댓글 불러오는 중...
댓글 쓰기...
이메일 (필수) 이름 (필수) 웹사이트
%d